Les nostres cèl·lules depenen de proteïnes que regulen tots els seus processos vitals. Les instruccions per produir aquestes proteïnes es troben al nostre material genètic, encriptades al codi de quatre lletres del DNA (A, C, G i T) en forma de gens. La causa de la gran majoria de patologies hereditàries, com pot ser la fibrosi quística o la predisposició a patir certs tipus de càncer, és l’acumulació en determinats gens de canvis en la seua seqüència de lletres (mutacions), que donen lloc a proteïnes defectuoses, causant la malaltia. Per tal de solucionar aquestes situacions hom podria pensar en transformar eixes proteïnes defectuoses en proteïnes funcionals. La manera de fer-ho és revertint les mutacions dels gens que les codifiquen. Però això és una tasca força complicada.
La dificultat per a modificar el genoma ve donada fonamentalment perquè les nostres cèl·lules s’esforcen per mantenir sempre una seqüència i nombre constant de gens. Per a aconseguir-ho disposen de mecanismes que reparen qualsevol dany o mutació produïts al DNA i d’altres que asseguren que cada cèl·lula rebrà la mateixa dosi genètica al final de mitosi (el procés pel qual la cèl·lula es divideix en dues cèl·lules idèntiques). Aquests són alguns dels punts de control que garanteixen la nostra supervivència. Tanmateix, aquests mecanismes de salvaguarda són els que han dificultat moltíssim la modificació dels nostres gens quan sí que ho volem fer.
Tots aquests entrebancs han limitat moltíssim el desenvolupament de teràpies gèniques, potser l’única possibilitat real avui en dia de curació de malalties genètiques hereditàries. Però sembla que l’avanç més gran i revolucionari en aquest camp se n’està beneficiant molt de la recerca bàsica, tantes vegades menyspreada. El sistema que us explique més avall el coneixem gràcies a científics que estudien aspectes bàsics sobre la immunitat dels bacteris. Sóc conscient de què llegir la paraula bacteri pot tenir connotacions negatives, sobretot si pensem per exemple en la pudor que poden arribar a fer quan proliferen i descomponen fem, o quan provoquen infeccions. Tanmateix, també podem pensar en els bacteris com aquelles cèl·lules que poblen els nostres intestins i ens ajuden a digerir els aliments que ingerim. I vet aquí que en aquestes línies us descriuré un altre tret positiu que ens ofereixen els bacteris i que podem utilitzar en el nostre benefici: el sistema CRISPR-Cas.
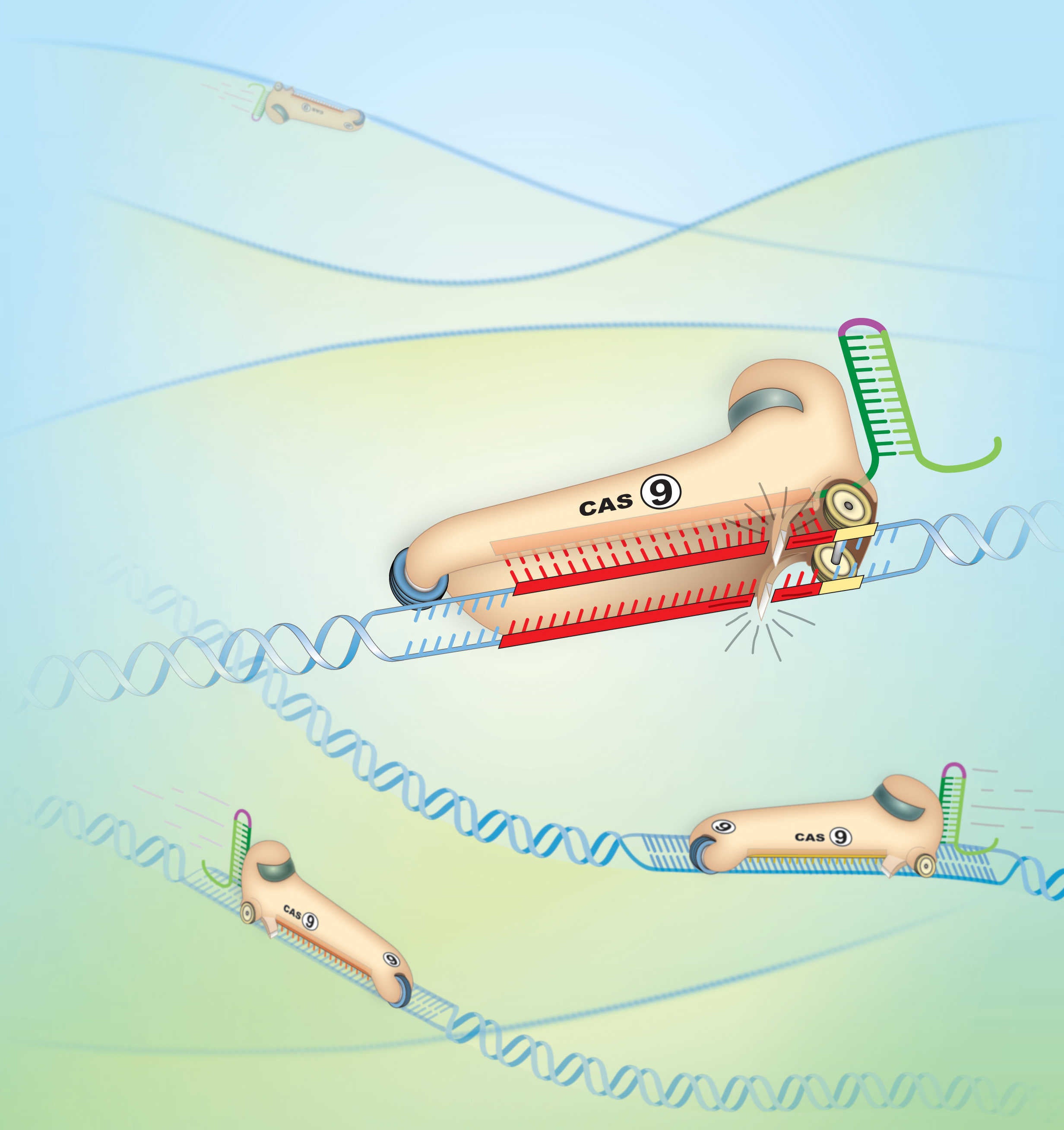
A l’any 2005 diversos grups d’investigació estudiant la immunitat bacteriana se n’adonaren de l’existència d’unes seqüències curtes i repetitives (CRISPR, per les seues sigles en anglès) presents tant al genoma d’eixos bacteris com al dels virus que els infectaven. Poc després es demostrava que hi havia gens associats als RNAs transcrits de les CRISPR, els Cas, que codificaven per a la producció de proteïnes que tallaven eixes seqüències dels virus. Així és com tot prenia sentit i es descobria que CRISPR-Cas era un mecanisme d’immunitat adaptativa: el bacteri “recordava” infeccions prèvies i produïa proteïnes que reconeixien i tallaven específicament el material genètic de nous virus atacants, impedint més infeccions. D’ençà aquells descobriments (fa poc més de 5 anys), s’ha desenvolupat un sistema simplificat per tal de reconèixer, tallar i modificar el genoma de qualsevol organisme de forma altament específica i molt més eficient que els mètodes utilitzats fins ara. L’avantatge més gran és que l’únic pas per construir el sistema CRISPR-Cas per al gen desitjat és la identificació d’una seqüència curta de RNA d’eixe gen (de 15 a 18 lletres de codi genètic) que s’associe a les proteïnes Cas. Una vegada produïts, els co-introduïm a les cèl·lules on volem revertir mutacions. Gràcies a programes d’ús gratuït que calculen quines són les millors seqüències per a cada gen aquest pas esdevé factible sense grans complicacions.
Aquest sistema ràpid, eficient, específic i barat, ha permès que diferents grups ja hagen aconseguit modificar la seqüència de 5 gens alhora en embrions de ratolins, modificar gens de plantes i de cèl·lules en cultiu (tant de cèl·lules troncals com diferenciades). I aquests són tan sols uns exemples. Moltes són les disciplines que se’n podran beneficiar de l’ús del sistema CRISPR-Cas, des de la medicina a l’agricultura, un benefici que repercuteix en sectors molt amplis de la societat.
Aquesta és sens dubte una història encoratjadora per a tots aquells que creuen en la ciència com motor del desenvolupament social i econòmic. És un exemple de com investigar qüestions bàsiques pot donar-nos solucions a problemes sofisticats. El divulgador científic Pere Estupinyà escrivia recentment que hem de fer ciència bàsica mirant a la seua aplicació futura per tal que siga productiva. Casos com CRISPR-Cas demostren que l’aplicació de vegades no es pot preveure fàcilment, però existeix. CRISPR-Cas demostra que la ciència bàsica és necessària i que amb imaginació i creativitat pot generar un coneixement aplicable en molts camps. Diverses companyies han fet ja de CRISPR el motor per créixer exponencialment.
Des que el descobriment inicial té lloc fins trobar-ne una aplicació sol ser un procés més llarg que posar en marxa un projecte en altres indústries més immediates. Per això cal tindre present que la inversió en ciència és a llarg termini, un termini de més de 4 anys, que és en el que acostuma a pensar la nostra classe política. Però tot i que la riquesa generada a partir del coneixement no és tan ràpida i temptadora com la de les bombolles que tan bé coneixem els valencians, sembla que s’assenta sobre unes bases molt més sòlides…